26年北京高考考试已经打响,为帮助考生更好的备考,北京高考考试在线团队整理了2026年北京高考考试化学知识性入门知识点,推荐给同学们学习。
选考科目备考,需要一些借用一些资料来提高科目成绩及择校选专业。因此,北京高考考试在线团队特意筹备了以下资料:
物理+化学+生物选科组合可报院校剖析:https://www.gaokzx.com/form?xyppid=575799726083938901
2020|2025年北京高考考试考试真题汇编:https://www.gaokzx.com/form?xyppid=575673408394631765
大家为大伙筹备了,推荐最新升学动态、政策、考试模拟试题、备考攻略等信息,一路伴随考生们备考。
扫描二维码进群

2026年北京高考考试化学知识性入门知识点
现代仪器
1.核磁共振仪:有机物中处于不同化学环境的氢原子类型;
2.红外光谱仪:主要测定有机物中官能团的类型;
3.紫外光谱仪:有机物中的共轭结构(主要指苯环);
4.质谱仪:有机物的相对分子水平,对测定结构也有肯定的帮忙;
5.原子吸收(发射)光谱仪:测定物质的的金属元素,也可测定非金属元素;
6.分光光度计:测定溶液中物质的成分以含量,重点是测反应速率;
7.色谱剖析仪:借助不同物质在固定相和流动相中分配比的不同,对物质进行离别,主要分类物理性质和化学性质相近的物质,纸层析就是其中的一种;
8.李比希燃烧法:测定有机物中C、H、O、N、Cl的有无及含量,CO2、H2O、N2、HCl;
9.铜丝燃烧法:测定有机物中是不是含卤素,火焰为绿色说明含有卤素;
10.钠熔法:测定有机物是不是含有X、N、S,NaX、Na2S、NaCN;
11.元素剖析仪:测定物质中元素的类型;
12.扫面隧道显微镜:察看、操纵物质表面的原子和分子;
化学史
1.道尔顿:提出原子学说;
2.汤姆生:在阴极射线实验基础上提出葡萄干面包式模型;
3.卢瑟福:在粒子散射实验基础上提出核+电子模型;
4.波尔:在量子力学基础上提出轨道模型;
5.舍勒:发现氯气;
6.维勒:人工合成尿素;
7.门捷列夫:元素周期表;
材料及成分
1. 火棉:纤维素与硝酸完全酯化的产物;
2. 胶棉:纤维素与硝酸不完全酯化的产物;
3. 人造丝、人造毛、黏胶、人造棉纤维、铜氨纤维主要成分都是纤维素;
4. 醋酸纤维:纤维素与醋酸酐酯化后的产物;
5. 光导纤维:成分为SiO2,全反射原理;
6. Al2O3:人造刚玉、红宝石、蓝宝石的主要成分;
7. SiO2:硅石、玻璃、石英、玛瑙、光纤的主要成分;
8. 硅酸盐:水泥、陶器、瓷器、琉璃的主要成分;
9. 新型无机非金属材料:氧化铝陶瓷、氮化硅陶瓷、碳化硼陶瓷、光纤等;具备耐高温、强度大的特质,还具备电学特质、光学特质、生物功能;
10. 传统无机非金属材料:水泥、玻璃、陶瓷;
11. 新型高分子材料:高分子膜、尿不湿、隐形眼镜、人造关节、心脏补片、液晶材料等;
12. 三大合成材料:合成塑料、合成纤维、合成橡胶;
能源问题
1.石油:烷烃、环烷烃、芳香烃的混合物
石油的分馏是物理变化,石油的裂化、裂解都是化学变化
2.煤:主要成分是碳
煤的干馏、气化、液化都是化学变化;
3.生物质能:通过光合用途,太阳能以化学能的形式贮藏在生物质中的能量形式;木材、森林废弃物、农业废弃物、植物、动物粪便、沼气等;
4.新能源:太阳能、风能、潮汐能、氢能、核能;
环境问题与食品安全
1.臭氧层空洞:氟利昂进入平流层致使臭氧降低;
2.温室效应:大方中CO2、CH4增多,导致全球平均气温上升;
3.光化学烟雾:NxOy在紫外线用途下发生一系列的光化学反应而生成的有毒气体;
4.赤潮:海水富营养化;
5.水华:淡水富营养化;
6.酸雨:pH<5.6;
7.室内污染:HCHO、苯、放射性氡、电磁辐射;
8.PM2.5:直径2.5m(2.510|6m)能在空中长期悬浮,颗粒小,表面积大,能吸附很多有害有毒物质(如金属、微生物);雾霾天气的形成于部分颗粒在空气中形成气溶胶有关
9.非法食品添加剂:吊白块、苏丹红、三聚氰胺、硼酸、荧光增白剂、瘦肉精、工业明胶;
10.腌制食品:腌制过程中会产生亚硝酸盐,具备致癌性;
11.地沟油:地沟油中有黄曲霉素,具备致癌性;可以制肥皂盒生物柴油;
12.绿色化学:绿色化学是指化学反应及其过程以原子经济性为基本原则,即在获得新物质的化学反应中充分借助参与反应的每一个材料原子,达成零排放。绿色化学的目的是研究和探寻能充分借助的无毒害材料,最大限度地节省能源,在化工生产的各环节都达成净化和无污染的反应渠道;
糖类
1. 单糖:
丙糖:甘油醛(最简单的糖)CH2(OH)CH(OH)CHO
戊糖:核糖、脱氧核糖;
己糖:葡萄糖、半乳糖、果糖;
2. 二糖:
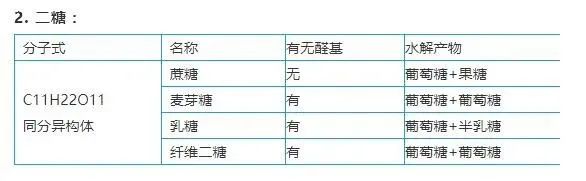
3. 多糖:
①淀粉(C6H10O5)n和纤维素(C6H10O5)n,n值是一个区间,故两者不是同分异构体,都是混合物;
②判断淀粉水解程度的办法 (在酸性条件下水解)
a.尚未水解:需要先加NaOH中和硫酸,再加入新制氢氧化铜加热,无砖红色沉淀;
b.完全水解:加入碘水,不呈蓝色
c.取两份,一份加入碘水呈蓝色;一份加入NaoH中中和硫酸后,再加入新制氢氧化铜加热,有砖红色沉淀
③人体中无纤维素酶,不可以消化纤维素,多吃含纤维素食物可促进肠道蠕动;
氨基酸和蛋白质
1.|氨基酸:氨基和羧基连在同一个碳上天然蛋白质水解生成的氨基酸都是.|氨基酸;
2.两性:|NH2具备碱性,|COOH具备酸性
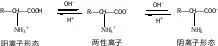
固体氨基酸主要以内盐形式存在,所以具备较高的熔沸点,且难溶于有机溶剂;
两个不一样的氨基酸缩合形成二肽,有四种不一样的产物(两个自己,两个交叉);
3.离别:当氨基酸以两性离子存在于溶液中时,其溶解度最小,而不一样的氨基酸出现这样的情况的pH各不相同,故可借助此差异,通过调节溶液的pH值来离别氨基酸;
4.盐析:很多蛋白质在水中有肯定的溶解度,溶于水形成胶体;在浓度较高的低盐金属盐(Na2SO4)或铵盐中,能破坏胶体结构而使蛋白质溶解度减少,从而使蛋白质变成沉淀析出,析出的蛋白质仍具备生物活性;
5.变质:
①重金属盐、强酸、强碱、甲醛、酒精等可使蛋白质变性而失去活性,析出的蛋白质不再溶于水;
②当人体误食重金属盐时,可喝很多的牛奶、豆奶、鸡蛋清来解毒;
③酒精消毒是破坏了病毒的蛋白质活性而杀死病毒;
6.颜色反应:
①蛋白质遇双缩脲试剂呈玫瑰紫色;
②含苯环的蛋白质与浓硝酸用途生成黄色物质;
③氨基酸遇茚三酮呈紫色;
7.氢键存在:
①蛋白质的二级结构;
②DNA双螺旋结构,AT之间两条,CG之间三条;
油脂
1.油脂不是高分子,是由高级脂肪酸与甘油形成的酯类;
2.油:不饱和脂肪酸甘油酯,常温液态,如豆油、花生油;能使溴水退色;不可以从溴水中萃取溴单质;
3.脂肪:饱和脂肪酸甘油酯,常温固态,如猪油、牛油油;
4.皂化反应:油脂与碱反应生成甘油与高级脂肪酸钠;
5.油脂硬化:不饱和高级脂肪酸甘油酯与氢气反应生成饱和高级脂肪酸甘油酯;
6.油脂和矿物油不是同一物质,矿物油是烃类;
7.天然的油脂都是混合物;
8.硬水中有较多的Mg2+、Ca2+,会生成不溶于水的(C17H35COO)2Mg和(C17H35COO)2Ca,使肥皂的消耗量增加,故不适合在硬水中用肥皂;
9.不饱和脂肪酸甘油酯中的双键会被空气氧化而变质;
10.地沟油和人造奶油都是油脂;
化学中的未必
1.原子核未必都是由质子和中子构成的。如氢的同位素(11H)中只有一个质子。
2.酸性氧化物未必都是非金属氧化物。如Mn2O7是HMnO4的酸酐,是金属氧化物。
3.非金属氧化物未必都是酸性氧化物。如CO、NO都不可以与碱反应,是不成盐氧化物。
4.金属氧化物未必都是碱性氧化物。如Mn2O7是酸性氧化物,Al2O3是两性氧化物。
5.电离出的阳离子都是氢离子的可能不是酸。如苯酚电离出的阳离子都是氢离子,属酚类,不是酸。
6.由同种元素组成的物质可能不是单质。如金刚石与石墨均由碳元素组成,二者混合所得的物质是混合物;由同种元素组成的纯净物是单质。
7.晶体中含有阳离子未必含有阴离子。如金属晶体中含有金属阳离子和自由电子,而无阴离子。
8.有单质参加或生成的化学反应可能不是氧化还原反应。如金刚石石墨,同素异形体间的转化因反应前后均为单质,元素的化合价没变化,是非氧化还原反应。
9.离子化合物中未必含有金属离子。如NH4Cl是离子化合物,其中不含金属离子。
10.与水反应生成酸的氧化物可能不是酸酐,与水反应生成碱的氧化物可能不是碱性氧化物。如NO2能与水反应生成酸硝酸,但不是硝酸的酸酐,硝酸的酸酐是N2O5,Na2O2能与水反应生成碱NaOH,但它不是碱性氧化物,是过氧化物。
11.pH=7的溶液可能不是中性溶液。只有在常温时水的离子积是110|14,此时pH=7的溶液才是中性。
12.用pH试纸测溶液的pH时,试纸用蒸馏水湿润,测得溶液的pH可能没有误差。
13.分子晶体中未必含有共价键。如稀少气体在固态时均为分子晶体,不含共价键。
14.能使品红溶液褪色的气体可能不是SO2,如Cl2、O3均能使品红溶液褪色。
15.金属阳离子被还原未必得到金属单质。如Fe3+可被还原为Fe2+。
16.某元素由化合态变为游离态时,该元素未必被还原。如2H2O=2H2+O2,氢元素被还原而氧元素被氧化。
17.强氧化物与强还原剂未必能发生氧化还原反应。如浓硫酸是容易见到的强氧化剂,氢气是容易见到的还原剂,但可用浓硫酸干燥氢气,因二者不发生反应。
18.放热反应在常温下未必比较容易发生,吸热反应在常温下未必不可以发生。如碳与氧气的反应为放热反应,但须点燃;Ba(OH)28H2O与NH4Cl反应为吸热反应,但在常温下比较容易发生。
19.含金属元素的离子未必都是阳离子。如AlO2|、MnO4|。
20.最外层电子数大于4的元素可能不是非金属元素。如周期表中ⅣA、ⅤA、ⅥA中的金属元素最外层电子数均多于4个。
21.不可以在强酸性溶液中很多存在的离子,未必能在强碱性溶液中很多存在。如HCO3|、HS|等离子既不可以在强酸性溶液中很多存在,也不可以在强碱性溶液中很多存在。
22.组成和结构一样的物质,相对分子水平越大,熔沸点未必越高。通常情况下该结论是正确的,但因H2O、HF、NH3等分子间能形成氢键,熔沸点均比同主族元素的氢化物高。
23.只由非金属元素组成的晶体未必是分子晶体。如NH4Cl是离子晶体。
24.只含有极性键的分子可能不是极性分子。如CCl4、CO2等都是含有极性键的非极性分子。
25.铁与强氧化性酸反应未必生成三价铁的化合物。铁与浓硫酸、硝酸等反应,若铁过量则生成亚铁离子。
26.强电解质未必导电;一般强电解质的晶体不导电;
27.强电解质的导电性未必强于弱电解质;与溶度有关;
28.失去电子难的原子获得电子的能力未必强。如稀少气体原子既不容易失去电子也不容易得到电子。
声明:本文由北京高考考试在线团队(官方公众号:bjgkzx)排版编辑,内容源自互联网,如有侵权,请准时联系管理员删除。

